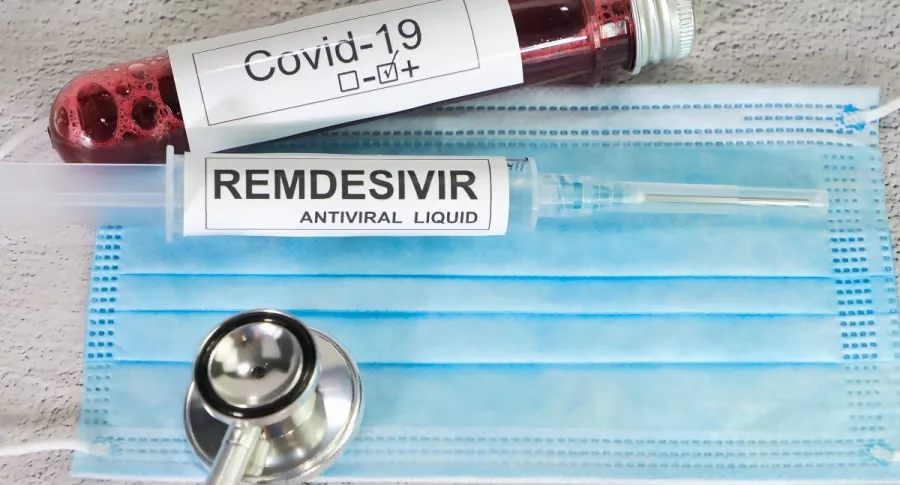
El laboratorio Gilead anunció que recibió la autorización para el medicamento y destacó que de momento se trata del único tratamiento específico contra el COVID-19 aprobado tras un proceso de verificación más riguroso y definitivo.
Otros tratamientos han recibido autorizaciones de utilización de urgencia, que son temporales y otorgadas en base a datos menos completos que una autorización plena, pero estas pueden ser revocadas al final del estado de urgencia sanitario.
Más tratamientos están disponibles desde hace meses en los hospitales gracias a las autorizaciones temporales, o porque son medicamentos relativamente banales, como el corticoide dexametasona.



El remdesivir fue uno de los primeros medicamentos que mostraron relativa eficacia en los rigurosos ensayos para acortar en varios días el tiempo de recuperación de los pacientes hospitalizados. Europa y otros países también lo autorizaron de forma temporal desde la primavera boreal, pero no se ha probado que reduzca la mortalidad.
El medicamento podrá darse a los adultos y a los niños de más de 12 años que pesen al menos 40 kilos, en caso de que requieran hospitalización, y solo podrá administrase por inyección, en un centro médico o entorno equivalente. Otra autorización de urgencia fue acordada paralelamente para los niños de menos de 12 años que pesen, al menos, 3,5 kilos.
El presidente estadounidense, Donald Trump, que enfermó de COVID-19 a comienzos de octubre, recibió este tratamiento durante cinco días, además de otros.
LO ÚLTIMO


.svg)