Mediante un comunicado, Allergan explicó que está tomando esta decisión “como medida de precaución después de la notificación recientemente sobre la incidencia poco frecuente de linfoma anaplásico de células grandes asociado” a sus implantes mamarios ‘BIOCELL’.
“La seguridad del paciente es una prioridad para Allergan. Se recomienda a los pacientes que hablen con su cirujano plástico sobre los riesgos y beneficios de su tipo de implante en caso de que tengan alguna duda”, añadió la empresa irlandesa.
Estos implantes ya han causado al menos 33 muertes, casi todas en Latinoamérica, debido a que en esta zona tiene una gran influencia. Tiene sedes en Colombia, Argentina, Bolivia, Brasil, Chile, Ecuador, Perú, Uruguay y Venezuela.
Países desarrollados como Francia, Canadá y Australia también fueron inundados con este tipo de producto en años anteriores, llegando a tener hasta el 80 % del mercado.
Las autoridades sanitarias de varios países se han dado cuenta desde 2011 de que algunos implantes estaban asociados a un alza de los linfomas anaplásicos de células grandes (LACG), un cáncer que se manifiesta a menudo por un derrame de líquido alrededor de la prótesis.


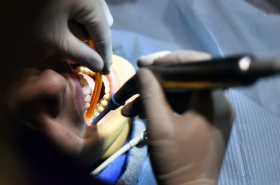

El mecanismo biológico que provoca esa enfermedad no ha sido identificado, pero se cree que el roce de la envoltura de los implantes contra los tejidos podría causar una inflamación.
Según los datos recogidos por la agencia federal de medicamentos (FDA), el 84 % de los 573 casos registrados en el mundo, a fecha de 6 de julio, están relacionados con implantes de ese fabricante.
La FDA contabilizó 33 fallecimientos en el mundo. De los 13 casos cuyos fabricantes conoce, 12 fueron de Allergan.
“Nuestro análisis muestra que el riesgo de LACG con implantes texturizados Biocell de Allergan es unas seis veces mayor que con implantes texturizados de otros fabricantes“, declaró la FDA en un comunicado.
“Aunque la incidencia total de LACG parece relativamente baja, una vez que los datos han señalado que el producto de un fabricante particular parece directamente vinculado a problemas graves en los pacientes, incluida la muerte, la FDA ha actuado para alertar a la compañía que nuevos datos mostraban la necesidad de una retirada”, indicó Amy Abernethy, portavoz de la FDA.
LO ÚLTIMO

.svg)