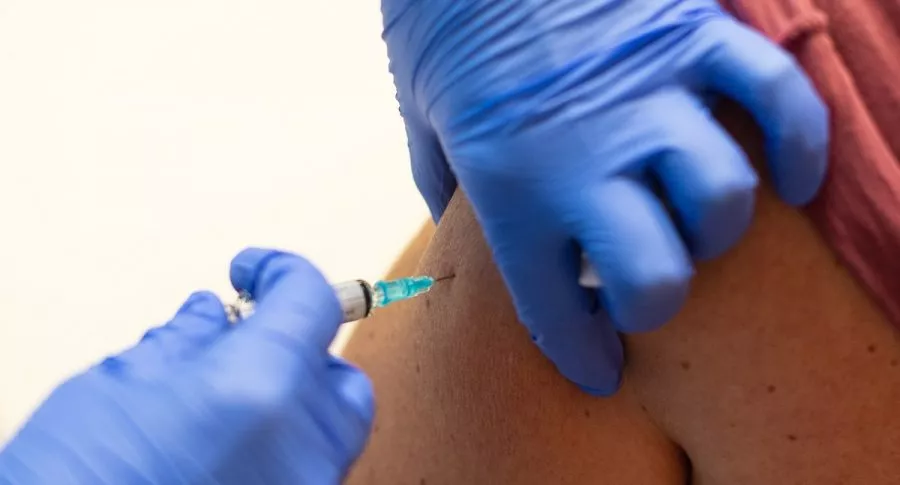
A través de un comunicado de prensa, Pfizer señaló este miércoles que su vacuna contra el coronavirus presenta una efectividad y seguridad del 95 %, 28 días después de la aplicación de la primera dosis.
“Los resultados del estudio marcan un paso importante en este histórico viaje de ocho meses para presentar una vacuna capaz de ayudar a poner fin a esta devastadora pandemia”, afirmó Albert Bourla, director ejecutivo de la compañía.
La farmacéutica, adicionalmente, enfatizó que cerca de 43.000 personas de todo el mundo han participado en los ensayos clínicos, de los cuales 41.000 recibieron la segunda dosis de la vacuna el pasado 13 de noviembre.
Aunque todavía faltan algunas pruebas, la compañía reiteró que el antídoto fue tolerado por todas las poblaciones, incluidos los ancianos (grupo de riesgo). Asimismo, indicó que los únicos efectos secundarios registrados fueron fatiga (3,8 %) y dolor de cabeza (2 %).
“La eficacia fue constante según la edad, género, raza y etnia. Además, la efectividad observada en adultos mayores de 65 años fue superior al 94 %. Con miles de personas infectadas todos los días, necesitamos urgentemente llevar una vacuna segura y eficaz”, concluyó Bourla.
Pfizer, por último, puntualizó en el comunicado que solicitará en los próximos días la respectiva autorización a la Administración de Alimentos y Medicamentos de Estados Unidos (FDA), para comercializar la vacuna contra el COVID-19.
Debido a este anunció, la compañía estadounidense abrió este miércoles con un alza en sus acciones del 4 %, mostrando una vez más que los mercados del mundo están respondiendo a este tipo de noticias.
BREAKING: We are proud to announce, along with @BioNTech_Group, that the Phase 3 study of our #COVID19 vaccine candidate has met all primary efficacy endpoints.
— Pfizer Inc. (@pfizer) November 18, 2020



Advertencia de la OMS, luego de noticia de la efectividad de vacunas contra el coronavirus
El director general de la Organización Mundial de la Salud (OMS), Tedros Adhanom Ghebreyesus, aseguró el pasado fin de semana que la llegada de las vacunas no terminará por el momento con la emergencia sanitaria.
“Seguimos recibiendo noticias alentadoras y continuamos siendo prudentemente optimistas. Por ahora, no es el momento de la complacencia. Tenemos una gran preocupación por el aumento del número de casos en algunos países”, precisó.
De las 48 vacunas experimentales contra el COVID-19 que actualmente se encuentran en ensayos clínicos en humanos, sólo once han entrado en la fase tres, antes de la homologación por las autoridades sanitarias.
Moderna, Pfizer, Sinovac, Sinopharm, Bharat Biotech, AstraZeneca, Johnson & Johnson, CanSino Biological, Sputnik V y Novavax son las 11 compañías que están en la última etapa de las investigaciones.
LO ÚLTIMO


.svg)